
Цезий.
Соединения цезия широко
распространены в природе, обычно в малых количествах совместно с соединениями
других щелочных металлов. Минерал поллуцит – силикат – содержит
34% оксида цезия Cs2O.
Элемент был открыт Р.Бунзеном методом спектроскопии в 1860. Основным применением
цезия является производство фотоэлементов и электронных ламп, один из
радиоактивных изотопов цезия Cs-137 применяется в лучевой терапии и научных
исследованиях.
Франций.
Последний член семейства
щелочных металлов франций настолько радиоактивен, что его нет в земной
коре в более чем следовых количествах. Сведения о франции и его соединениях
основаны на исследовании ничтожного его количества, искусственно полученного
(на высокоэнергетическом ускорителе) при a-распаде
актиния-227. Наиболее долгоживущий изотоп 22387Fr
распадается за 21 мин на 22388Ra
и b-частицы.
Согласно приблизительной оценке, металлический радиус франция составляет
2,7 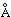 .
Франций обладает большинством свойств, характерных для других щелочных
металлов, и отличается высокой электронодонорной активностью. Он образует
растворимые соли и гидроксид. Во всех соединениях франций проявляет степень
окисления I. .
Франций обладает большинством свойств, характерных для других щелочных
металлов, и отличается высокой электронодонорной активностью. Он образует
растворимые соли и гидроксид. Во всех соединениях франций проявляет степень
окисления I.
ПОДГРУППА IIA
БЕРИЛЛИЙ, МАГНИЙ И ЩЕЛОЧНОЗЕМЕЛЬНЫЕ
МЕТАЛЛЫ – КАЛЬЦИЙ, СТРОНЦИЙ, БАРИЙ, РАДИЙ
Строго говоря, эта подгруппа состоит
из двух типов элементов. Бериллий и магний – элементы коротких периодов
– более сходны между собой, чем с другими четырьмя элементами, которые
собственно и образуют семейство щелочноземельных металлов. Фактически,
бериллий и в меньшей степени магний более сходны с первыми элементами
подгруппы IIIA.
Особенностью электронного строения любого
элемента подгруппы IIA является наличие двух электронов на внешнем слое
и внутренняя электронная структура по типу предыдущего благородного газа.
Способность отдавать два внешних валентных электрона возрастает в подгруппе
с увеличением атомного радиуса и атомного номера элемента. Максимальная
степень окисления составляет II, но имеются сведения о существовании соединений
со степенью окисления I. Такие соединения неустойчивы и диспропорционируют
с образованием свободного металла и иона М(II).
Физические
и химические свойства.
Все элементы подгруппы IIA
химически активны и поэтому в
свободном состоянии в природе не существуют. Щелочноземельные металлы
энергично реагируют с водой, вытесняя водород и образуя гидроксиды, как
и щелочные металлы. Магний взаимодействует только с кипящей водой, а бериллий
не реагирует даже с парами при высокой температуре. Бериллий отличается
от остальных элементов подгруппы и даже от магния по химическим и многим
физическим свойствам. Такое отличие характерно для всех элементов, начинающих
подгруппы А, что объясняется малым радиусом иона и соответственно высокой
зарядовой плотностью. Особенности и отличия свойств бериллия приведены
ниже.
назад
дальше
|


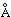 .
Франций обладает большинством свойств, характерных для других щелочных
металлов, и отличается высокой электронодонорной активностью. Он образует
растворимые соли и гидроксид. Во всех соединениях франций проявляет степень
окисления I.
.
Франций обладает большинством свойств, характерных для других щелочных
металлов, и отличается высокой электронодонорной активностью. Он образует
растворимые соли и гидроксид. Во всех соединениях франций проявляет степень
окисления I.