
Общие
свойства.
Сначала рассматриваются
некоторые общие свойства, затем свойства по подгруппам и отдельные элементы
более детально. Общие и физические свойства сведены в таблицы.
Электронная
конфигурация.
За некоторым исключением
все переходные элементы имеют 2 электрона на внешнем или высшем энергетическом
уровне и один или более электронов на низшем (n
– 1) или (n
– 2). При переходе от элемента к элементу в пределах одного ряда
элементов ядро увеличивается на 1 протон, увеличивая заряд, и соответственно
число электронов также увеличивается на 1. Этот дополнительный электрон
располагается на (n
– 1) или (n
– 2) уровне, т.е. на внутренней оболочке, что приводит к некоторому
уменьшению радиуса атома, или сжатию с увеличением атомного номера. На
основании этого эффекта можно объяснить многие периодические изменения
свойств.
Образование
связи.
Описанное электронное
строение позволяет всем этим элементам образовывать химическую связь в
соединениях с участием 3 электронов; многие переходные элементы образуют
связь с помощью 2 внешних электронов, и все эти элементы могут (хотя и
не всегда) предоставлять количество электронов, равное номеру группы,
в которой находится данный элемент. Возможность участия в связеобразовании
различного числа электронов называется поливалентностью. Например, у марганца,
элемента подгруппы VIIВ, степень окисления изменяется от II (MnCl2)
до VII (KMnO4).
Чем больше электронов участвует в образовании химической связи, тем более
ковалентной становится связь.
Окраска
ионов.
Так как при переходе
от одного элемента к другому вдоль ряда переходных элементов в периодической
таблице последующие электроны поступают на внутреннюю оболочку и поэтому
мало энергетически отличаются друг от друга, то достаточно небольших затрат
энергии для перескока электрона в более высокое энергетическое состояние.
Атомы и ионы, которые имеют такие подвижные электроны, обычно хорошо окрашены,
так как энергии света достаточно для перескока электронов. Поэтому многие
ионы переходных элементов окрашены и образуют окрашенные соединения.
Физические
свойства.
Малое количество электронов
на внешнем уровне объясняет высокую электро- и теплопроводность переходных
металлов. Те же электроны могут участвовать и в образовании связей между
атомами одного элемента. Природа такого связеобразовании не всегда понятна,
но коррелирует с высокими величинами температур плавления и кипения. Строгой
тенденции внутри семейства переходных металлов не существует, но атом
третьего члена подгруппы В не должен быть больше атома стоящего над ним
металла. Например, атомный радиус Zr равен 1,57 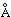 ,
а третий член подгруппы IVB
– Hf, стоящий под Zr, также имеет r
= 1,57 ,
а третий член подгруппы IVB
– Hf, стоящий под Zr, также имеет r
= 1,57 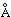 . .
назад
дальше
|


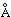 ,
а третий член подгруппы IVB
– Hf, стоящий под Zr, также имеет r
= 1,57
,
а третий член подгруппы IVB
– Hf, стоящий под Zr, также имеет r
= 1,57