
Получение.
Большое
промышленное значение галогенов предъявляет определенные требования к
методам их производства. С учетом разнообразия и сложности методов получения
существенное значение имеют расход и стоимость электроэнергии, сырья и
потребности в побочных продуктах.
Фтор.
Из-за
химической агрессивности фторид- и хлорид-ионов эти элементы получают
электролитическим путем. Фтор получают из флюорита: CaF2
при обработке серной кислотой образует HF (плавиковая кислота); из HF
и KF синтезируют KHF2,
который и подвергают электролитическому окислению в электролизере с раздельными
анодным и катодным пространствами, со стальным катодом и угольным анодом;
на аноде выделяется фтор F2,
а на катоде – побочный продукт водород, который следует изолировать
от фтора во избежание взрыва. Для синтеза таких важных соединений, как
полифторуглеводороды, в электролизере выделяющимся фтором фторируют органические
соединения, благодаря чему не требуются изоляция и накапливание фтора
в отдельных емкостях.
Хлор
производят
в основном из рассола NaCl в электролизерах с отделенным анодным пространством
для предотвращения реакции хлора с другими продуктами электролиза: NaOH
и H2;
таким образом, в результате электролиза получается три важных промышленных
продукта – хлор, водород и щелочь. Для осуществления этого процесса
используют различные модификации электролизеров. Хлор получается и как
побочный продукт при электролитическом производстве магния из MgCl2.
Б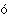 льшая
часть хлора используется для синтеза HCl по реакции с природным газом,
а HCl расходуется для получения MgCl2
из MgO. Хлор образуется
и в металлургии натрия из NaCl, однако метод электролиза из рассола дешевле.
В лабораториях промышленно развитых стран производят многие тысячи тонн
хлора по реакции 4HCl + MnO2
= MnCl2
+ 2H2O
+ Cl2. льшая
часть хлора используется для синтеза HCl по реакции с природным газом,
а HCl расходуется для получения MgCl2
из MgO. Хлор образуется
и в металлургии натрия из NaCl, однако метод электролиза из рассола дешевле.
В лабораториях промышленно развитых стран производят многие тысячи тонн
хлора по реакции 4HCl + MnO2
= MnCl2
+ 2H2O
+ Cl2.
Бром
получают
из скважин с рассолом, которые содержат больше бромид-ионов, чем морская
вода, являющаяся вторым по значимости источником брома. Бромид-ион легче
превращается в бром, чем фторид- и хлорид-ионы в аналогичных реакциях.
Поэтому для получения брома используют, в частности, хлор в качестве окислителя,
так как активность галогенов в группе убывает сверху вниз и каждый ранее
стоящий галоген вытесняет последующий. В производстве брома рассолы или
морскую воду предварительно подкисляют серной кислотой, а затем обрабатывают
хлором по реакции
2Br–
+ Cl2
® Br2
+ 2Cl–
Бром
выделяют из раствора выпариванием или продувкой с последующим его поглощением
разными реагентами в зависимости от дальнейшего применения. Например,
при реакции с нагретым раствором карбоната натрия получают кристаллические
NaBr и NaBrO3;
при подкислении смеси кристаллов бром регенерируется, обеспечивая не прямой,
но удобный метод накопления (хранения) этой коррозионно-активной с неприятным
запахом ядовитой жидкости. Бром можно также поглощать раствором SO2,
в котором образуется HBr. Из этого раствора бром легко выделить, пропуская
хлор (например, с целью проведения реакции брома с этиленом C2H4
для получения дибромэтилена C2H4Br2,
который используется как антидетонатор бензинов). Мировое производство
брома составляет свыше 300 000 т/год.
назад
дальше
|


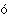 льшая
часть хлора используется для синтеза HCl по реакции с природным газом,
а HCl расходуется для получения MgCl2
из MgO. Хлор образуется
и в металлургии натрия из NaCl, однако метод электролиза из рассола дешевле.
В лабораториях промышленно развитых стран производят многие тысячи тонн
хлора по реакции 4HCl + MnO2
= MnCl2
+ 2H2O
+ Cl2.
льшая
часть хлора используется для синтеза HCl по реакции с природным газом,
а HCl расходуется для получения MgCl2
из MgO. Хлор образуется
и в металлургии натрия из NaCl, однако метод электролиза из рассола дешевле.
В лабораториях промышленно развитых стран производят многие тысячи тонн
хлора по реакции 4HCl + MnO2
= MnCl2
+ 2H2O
+ Cl2.