
Полоний.
Несмотря на ограниченное
количество полония, химия этого последнего элемента подгруппы VIA изучена
относительно неплохо благодаря использованию его свойства радиоактивности
(обычно в химических реакциях он смешивается с теллуром как носителем
или сопутствующим реагентом). Период полураспада наиболее устойчивого
изотопа 210Po
составляет всего 138,7 сут, поэтому понятны трудности его изучения. Для
получения 1 г Po требуется переработать более 11,3 т урановой смолки.
210Po
можно получить нейтронной бомбардировкой 209Bi,
который сначала переходит в 210Bi,
а затем выбрасывает b-частицу,
образуя 210Po.
По-видимому, полоний проявляет такие же степени окисления, как и другие
халькогены. Синтезированы гидрид полония H2Po,
оксид PoO2,
известны соли со степенями окисления II и IV. Очевидно, PoO3
не существует.
ПОДГРУППА VIIA. ГАЛОГЕНЫ
ФТОР, ХЛОР, БРОМ, ИОД, АСТАТ
Галогены
и особенно фтор, хлор и бром имеют большое значение для промышленности
и лабораторной практики как в свободном состоянии, так и в виде различных
органических и неорганических соединений. Фтор – бледножелтый высокореакционноспособный
газ, вызывающий раздражение дыхательных путей и коррозию материалов. Хлор
– тоже едкий, химически агрессивный газ темного зеленовато-желтого
цвета – менее реакционноспособен по сравнению со фтором. Он широко
используется в малых концентрациях для дезинфекции воды (хлорирование),
а в больших концентрациях ядовит и вызывает сильное раздражение дыхательных
путей (газообразный хлор применяли как химическое оружие в Первой мировой
войне). Бром – тяжелая красно-коричневая жидкость при обычных условиях,
но легко испаряется, превращаясь в едкий газ. Иод – темнофиолетовое
твердое вещество, легко сублимирующееся. Астат – радиоактивный элемент,
единственный галоген, не имеющий стабильного изотопа.
В семействе этих элементов по сравнению
с другими А-подгруппами наиболее выражены неметаллические свойства. Даже
тяжелый иод – типичный неметалл. Первый член семейства, фтор, проявляет
«сверхнеметаллические» свойства. Все галогены – акцепторы электронов,
и у них сильно выражена тенденция к завершению октета электронов путем
принятия одного электрона. Реакционная способность галогенов уменьшается
с ростом атомного номера, и в целом свойства галогенов изменяются в соответствии
с их положением в периодической таблице. В табл. 8а приведены некоторые
физические свойства, позволяющие понять отличия и закономерность изменения
свойств в ряду галогенов. Фтор проявляет во многом необычные свойства.
Например, установлено, что сродство к электрону у фтора не так высоко,
как у хлора, а это свойство должно указывать на способность принимать
электрон, т.е. на химическую активность. Фтор же ввиду очень малого радиуса
и близости валентной оболочки к ядру должен обладать наивысшим сродством
к электрону. Это несоответствие, по крайней мере отчасти, объясняется
необычно малой энергией связи F–F по сравнению с этой величиной
для Cl–Cl (см.
энтальпию диссоциации в табл. 8а). Для фтора она равна 159 кДж/моль, а
для хлора 243 кДж/моль. Из-за малого ковалентного радиуса фтора близость
неподеленных электронных пар в структуре :F:F: определяет легкость разрыва
этой связи. Действительно, фтор химически более активен, чем хлор, благодаря
легкости образования атомарного фтора. Величина энергии гидратации (см.
табл. 8а) указывает на высокую реакционную способность фторид-иона: ион
F–
гидратируется с б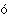 льшим
энергетическим эффектом, чем другие галогены. Маленький радиус и соответственно
более высокая зарядовая плотность объясняют б льшим
энергетическим эффектом, чем другие галогены. Маленький радиус и соответственно
более высокая зарядовая плотность объясняют б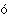 льшую
энергию гидратации. Многие необычные свойства фтора и фторид-иона становятся
понятными при учете размера и заряда иона. льшую
энергию гидратации. Многие необычные свойства фтора и фторид-иона становятся
понятными при учете размера и заряда иона.
Таблица
8а. ФТОР, ХЛОР, БРОМ, ИОД, АСТАТ
назад
дальше
|


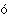 льшим
энергетическим эффектом, чем другие галогены. Маленький радиус и соответственно
более высокая зарядовая плотность объясняют б
льшим
энергетическим эффектом, чем другие галогены. Маленький радиус и соответственно
более высокая зарядовая плотность объясняют б