ХИМИЧЕСКИЕ СВЯЗИ, ФОРМУЛЫ И УРАВНЕНИЯ
Элементы, не обладающие стабильной электронной конфигурацией инертных газов, стремятся приобрести ее, вступая в химические реакции. Атомы, которым до стабильной конфигурации не хватает незначительного числа электронов или, напротив, у которых имеется небольшой их избыток, обычно образуют электрически заряженные частицы – ионы. Положительно заряженные ионы (образующиеся при потере электронов) называют катионами, отрицательно заряженные ионы (образующиеся при приобретении электронов) – анионами. Заряд ионов редко превышает 3, т.е. атомы редко теряют или приобретают более трех электронов. Атом натрия (см. схему), соединяясь с атомом хлора, теряет один наружный электрон и превращается в катион, а атом хлора приобретает этот электрон и становится анионом. Их внешние электронные оболочки становятся заполненными и содержат по восемь электронов. Катион и анион притягиваются, образуя хлорид натрия.

Электроны внешней оболочки, участвующие в образовании химических связей, называют валентными. (Валентность элемента равна числу связей, которые он способен образовать.) Некоторые элементы и их валентные электроны перечислены в приведенной выше таблице. В ней также указаны атомные номера элементов и наиболее распространенные ионы. Элементы, имеющие одинаковую электронную конфигурацию внешних оболочек и обладающие сходными физическими и химическими свойствами, объединены в периодической системе элементов в группы от I до VIII, причем номер группы совпадает с числом валентных электронов.
Периодическая система элементов помогает понять, чем объясняется сходство элементов, принадлежащих данной группе, и почему эти элементы все-таки отличаются друг от друга. Открытие периодического закона и публикация периодической системы русским химиком Д.И.Менделеевым в 1869 явились важнейшим этапом в систематизации свойств известных и предсказании еще неоткрытых химических элементов. См. также ПЕРИОДИЧЕСКАЯ СИСТЕМА ЭЛЕМЕНТОВ.
Ионная связь.
Противоположно заряженные ионы притягиваются друг к другу и сближаются, но лишь до определенного предела. Когда расстояние между ионами становится слишком мало, их электронные облака начинают отталкиваться, и дальнейшее сближение становится невозможно. Таким образом, есть определенное расстояние, на котором ионная пара наиболее стабильна. Его называют длиной ионной связи. Пространственное расположение заряженных частиц в веществе, имеющем ионный характер состояния, строго упорядоченно. В качестве примера ионных соединений можно привести обычную поваренную соль NaCl, в которой ион натрия Na+ связан с ионом хлора Cl–, или хлорид кальция CaCl2 с соотношением между ионами кальция Са2+ и хлорид-ионами Cl– 1:2. Как NaCl, так и CaCl2 электрически нейтральны.
Ковалентная связь.
Другой распространенный тип связи – ковалентная связь – возникает, когда два атома обобществляют одну (или более) пару электронов. При образовании ковалентной связи атомы удерживаются вместе электростатическим притяжением ядер к общей электронной паре, в отличие от ионной связи, в основе которой лежит электростатическое притяжение между самими ионами. Ковалентные связи обычно образуются в тех случаях, когда ядра атомов притягивают электроны примерно с одинаковой силой. Такая связь существует, например, в молекуле хлора (см. схему). Есть удобное правило для определения типа связи между атомами двух элементов: если один элемент находится в левой части периодической таблицы, а другой – в правой, то связь между ними будет ионной (см. элементы, перечисленные в приведенной выше таблице).

Если валентные электроны обозначить точками, то различие между двумя типами связи станет более наглядным:

Соединения типа LiF, BeO или BeF2 ионные. Соединения, молекулы которых состоят из элементов – соседей по периодической таблице, как правило, ковалентные (CO2, CF4, NO2, N2, O2, F2). Правда, некоторые металлы образуют как ионные, так и ковалентные соединения.
Два атома могут иметь две или даже три общие электронные пары, образуя двойную или тройную связь:
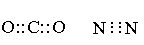
назад
дальше
|